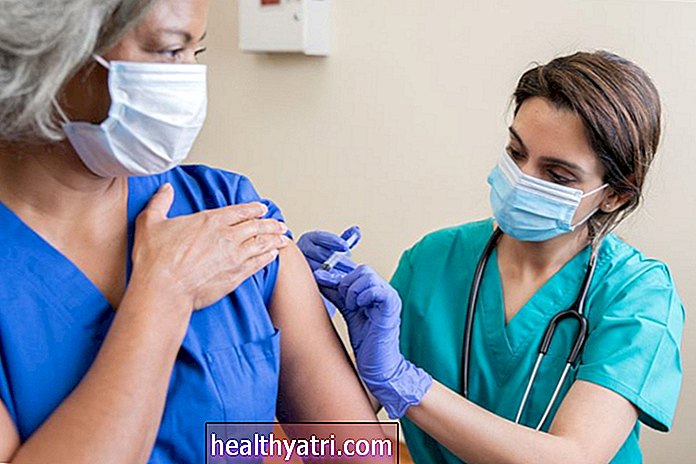
รูปภาพ Sasiistock / Getty
ประเด็นที่สำคัญ
- ไฟเซอร์ได้รับการอนุมัติจาก FDA ให้เริ่มทดสอบวัคซีนป้องกันไวรัสโคโรนาในเด็กอายุ 12 ปีขึ้นไป
- ผู้เชี่ยวชาญกล่าวว่าการรวมเด็กในการทดลองทางคลินิกมีความสำคัญต่อการพัฒนาโดยรวมของวัคซีนที่จะป้องกันทั้งเด็กและผู้ใหญ่จาก COVID-19
- ตามเว็บไซต์ของ บริษัท ไฟเซอร์ได้ลงทะเบียนอาสาสมัครมากกว่า 39,000 คนในการศึกษาแล้ว อาสาสมัครมากกว่า 34,000 คนได้รับการฉีดวัคซีนครั้งที่สองแล้ว
ไฟเซอร์ บริษัท ยาของสหรัฐอเมริกาประกาศในเดือนตุลาคมว่า บริษัท ได้รับอนุญาตจากสำนักงานคณะกรรมการอาหารและยาของสหรัฐอเมริกา (FDA) ให้เริ่มลงทะเบียนเด็กที่อายุน้อยกว่า 12 ปีในการทดลองวัคซีนโคโรนาไวรัส
“ ด้วยการทำเช่นนั้นเราจะสามารถเข้าใจถึงความปลอดภัยและประสิทธิภาพของวัคซีนที่อาจเกิดขึ้นได้ดีขึ้นในแต่ละบุคคลที่มีอายุและภูมิหลังมากขึ้น” บริษัท กล่าวในแถลงการณ์ฉบับปรับปรุง
นี่จะเป็นการทดลองวัคซีน COVID-19 ครั้งแรกในสหรัฐอเมริกาที่รวมเด็กไว้ด้วย ในเดือนตุลาคมไฟเซอร์เป็นหนึ่งในสี่ บริษัท ของสหรัฐอเมริกาที่มีวัคซีนในการทดลองทางคลินิกระยะที่ 3
ไฟเซอร์ได้ขยายระยะที่ 3 ของการทดลองเพื่อรวมเด็กอายุ 16 ปีขึ้นไปตลอดจนผู้ที่เป็นโรคภูมิคุ้มกันบกพร่องของมนุษย์ (HIV) เรื้อรังไวรัสตับอักเสบซีและไวรัสตับอักเสบบี
ทำไมต้องทดสอบวัคซีน COVID-19 ในเด็ก
ก่อนที่ไฟเซอร์จะได้รับการอนุมัติให้เริ่มทำการทดสอบในเด็กผู้เชี่ยวชาญได้ตีพิมพ์รายงานในวารสารโรคติดเชื้อทางคลินิกระบุความสำคัญของการทดสอบดังกล่าว
“ ผลกระทบโดยตรงจาก COVID-19 ต่อเด็กนั้นมากกว่าที่พบในเชื้อโรคอื่น ๆ ซึ่งตอนนี้เรามีวัคซีนสำหรับเด็กที่มีประสิทธิภาพแล้ว” รายงานระบุ “ นอกจากนี้บทบาทของเด็กในการแพร่เชื้อ SARS-CoV-2 ยังไม่ได้รับการยอมรับอย่างชัดเจน การทดลองทางคลินิกระยะที่ 2 อย่างรอบคอบสามารถจัดการกับข้อกังวลด้านความปลอดภัยของวัคซีน COVID-19 ที่อาจเกิดขึ้นได้อย่างเพียงพอ”
สุซานฟามนพ
เราไม่สามารถเอาชนะการแพร่กระจายของไวรัสนี้ได้เว้นแต่เราจะฉีดวัคซีนให้ลูก
- สุซานฟามนพSharon Nachman หัวหน้าแผนกโรคติดเชื้อในเด็กที่โรงพยาบาลเด็ก Stony Brook ในนิวยอร์กเห็นด้วยกับรายงานโดยบอก Verywell ว่า“ กุมารแพทย์สนใจที่จะดูรายละเอียดของการศึกษาและวิธีการฉีดวัคซีนในเด็ก .”
มีประโยชน์เฉพาะในการทดสอบวัคซีนในเด็กตามที่ Nachman กล่าว นักวิจัยจะสามารถประเมินการตอบสนองของระบบภูมิคุ้มกันในระยะสั้นและระยะยาวซึ่งรวมถึงการหาว่าปริมาณวัคซีนที่ใช้ในผู้ใหญ่นั้นจำเป็นสำหรับเด็กหรือไม่หรือพวกเขาจะมีการตอบสนองของระบบภูมิคุ้มกันที่คล้ายคลึงกันกับขนาดที่ต่ำกว่า
Nachman กล่าวว่าสิ่งสำคัญเช่นกันที่ต้องทราบว่าเนื่องจาก coronavirus ในผู้ใหญ่สามารถนำหน้าด้วยการสัมผัสกับการติดเชื้อที่ไม่มีอาการในเด็กการสร้างวัคซีนเพื่อรักษาทั้งครอบครัวอาจ "ช่วยลดการแพร่เชื้อที่บ้านและในชุมชนได้อีกไกล"
Suzanne Pham, MD, รองหัวหน้าเจ้าหน้าที่การแพทย์ของโรงพยาบาล Weiss Memorial ในชิคาโกกล่าวกับ Verywell ว่ายิ่งเด็กได้รับวัคซีนเร็วเท่าไหร่อัตราการแพร่เชื้อที่เร็วขึ้นก็จะลดลง
“ การฉีดวัคซีนให้เด็กอย่างมีประสิทธิภาพความเสี่ยงของเด็กที่แพร่เชื้อไวรัสภายในชุมชนจะลดน้อยลงโดยเฉพาะอย่างยิ่งกับผู้ที่มีความเสี่ยงสูงที่อ่อนแอต่อการเจ็บป่วยขั้นรุนแรงหรือขั้นวิกฤต” ฟามกล่าวกับเวลล์เวลล์ “ สิ่งนี้จะช่วยให้โรงเรียนสามารถเริ่มเปิดได้อีกครั้งและกิจกรรมที่สำคัญสำหรับการพัฒนาเด็กของเราให้กลับมาดำเนินการต่อในรูปแบบที่มีการควบคุม เราไม่สามารถเอาชนะการแพร่กระจายของไวรัสนี้ได้เว้นแต่เราจะฉีดวัคซีนให้ลูก เราต้องมีภูมิคุ้มกันฝูงเพียงพอในสังคมจึงจะสามารถป้องกันการแพร่ระบาดได้”
วัคซีน COVID-19: ติดตามว่ามีวัคซีนชนิดใดบ้างใครสามารถรับวัคซีนได้บ้างและปลอดภัยเพียงใด
การทดลองวัคซีนเริ่มต้นอย่างไร?
Pham อธิบายว่าสำหรับวัคซีนที่จะทดสอบในผู้ใหญ่หรือเด็ก บริษัท จะต้องส่งใบสมัคร Investigational New Drug (IND) ไปยัง FDA ก่อน
แอปพลิเคชันจะอธิบายถึงวัคซีนวิธีการผลิตและการทดสอบการควบคุมคุณภาพที่ต้องใช้ แอปพลิเคชันนี้ยังรวมถึงข้อมูลจากการทดสอบในสัตว์ที่แสดงให้เห็นว่าวัคซีนมีความปลอดภัยสำหรับการทดสอบเบื้องต้นในมนุษย์
ตามที่ FDA อธิบายขั้นตอนการสมัครมีหลายขั้นตอน:
ในระหว่างการพัฒนาพรีคลินิกในช่วงต้นของยาตัวใหม่เป้าหมายหลักของผู้สนับสนุนคือการพิจารณาว่าผลิตภัณฑ์มีความปลอดภัยพอสมควรสำหรับการใช้งานครั้งแรกในมนุษย์หรือไม่และสารประกอบดังกล่าวมีฤทธิ์ทางเภสัชวิทยาที่แสดงถึงการพัฒนาเชิงพาณิชย์หรือไม่
เมื่อผลิตภัณฑ์ได้รับการระบุว่าเป็นผลิตภัณฑ์ที่เหมาะสมสำหรับการพัฒนาในขั้นต่อไปผู้สนับสนุนจะมุ่งเน้นไปที่การรวบรวมข้อมูลและข้อมูลที่จำเป็นเพื่อกำหนดว่าผลิตภัณฑ์จะไม่ทำให้มนุษย์ได้รับความเสี่ยงที่ไม่สมเหตุสมผลเมื่อใช้ในการศึกษาทางคลินิกในระยะเริ่มแรกที่ จำกัด
จากนั้นวัคซีนจะได้รับการทดลองระยะที่ 1 ซึ่ง Pham อธิบายว่า“ การศึกษาความปลอดภัยและการสร้างภูมิคุ้มกันในมนุษย์จำนวนน้อยที่ได้รับการตรวจสอบอย่างใกล้ชิด”
“ ระยะที่ 2 ประกอบด้วยการศึกษาขนาดยาและขยายไปสู่อาสาสมัครที่เป็นมนุษย์จำนวนมากขึ้น (หลายร้อย) ราย” ฟามกล่าว “ จากนั้นการทดลองระยะที่ 3 พยายามลงทะเบียนอาสาสมัครหลายพันคนเพื่อจัดทำเอกสารประสิทธิผลและดูข้อมูลด้านความปลอดภัยต่อไป”
ตามเว็บไซต์ของ บริษัท ไฟเซอร์ได้ลงทะเบียนอาสาสมัครมากกว่า 39,000 คนในการศึกษา มากกว่า 34,000 คนได้รับวัคซีนครั้งที่สอง
สิ่งนี้หมายถึงอะไรสำหรับคุณ
การทดลองทางคลินิกระยะที่ 3 ซึ่งรวมถึงการทดสอบวัคซีน COVID-19 ในเด็กเป็นสัญญาณของความคืบหน้า อย่างไรก็ตามไม่สามารถรีบฉีดวัคซีนได้ การสรุปผลต้องใช้เวลาในการปกป้องความปลอดภัยของผู้เข้าร่วมการทดลองเช่นเดียวกับผู้ใหญ่และเด็กที่จะได้รับวัคซีนรุ่นสำเร็จรูปในที่สุด